Durante décadas, o tratamento dos gliomas difusos de grau 2 (os chamados “baixo grau”) foi uma balança difícil: adiar radioterapia e quimioterapia para preservar a cognição e qualidade de vida, mas sem abrir mão do controle tumoral. Para muitos pacientes, o caminho era previsível: cirurgia → observação (ou RT/QT em casos selecionados) → progressão → nova intervenção.
A chegada do vorasidenibe (nome comercial em vários países: VORANIGO®) inaugura um novo capítulo porque, pela primeira vez, temos uma terapia-alvo oral, penetrante no sistema nervoso central, que atua no evento molecular fundador de grande parte desses tumores: a mutação em IDH1/IDH2.
1) Relembrando o essencial: o que significa “glioma IDH-mutante”?
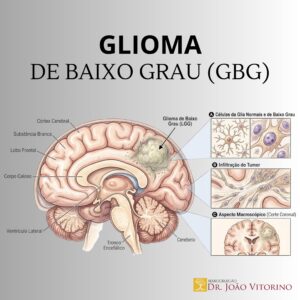
As mutações em isocitrato desidrogenase (IDH1 ou IDH2) são típicas de muitos astrocitomas e oligodendrogliomas de grau 2. Elas não são um detalhe de laboratório: representam uma alteração metabólica que muda a biologia do tumor.
A peça central: o 2-hidroxiglutarato (2-HG)
Quando o IDH está mutado, a enzima passa a produzir 2-hidroxiglutarato (2-HG), um “oncometabólito” que interfere em mecanismos de regulação epigenética e diferenciação celular. Em termos simples: o tumor ganha vantagens para persistir e evoluir ao longo do tempo.
Esse raciocínio leva a uma pergunta direta: se bloquearmos o IDH mutante, conseguimos desacelerar a história natural do tumor?
O vorasidenibe foi desenhado para responder exatamente isso.
2) O que é o Vorasidenibe e por que ele é diferente?
O vorasidenibe é um inibidor dual de IDH1 e IDH2 mutantes com uma característica crucial para tumores cerebrais: ele atravessa bem a barreira hematoencefálica (brain-penetrant). Na prática, isso é o que separa muitos fármacos “promissores” de uma terapia realmente efetiva no SNC.
Mecanismo em uma frase
Inibe IDH1/IDH2 mutantes → reduz 2-HG → desacelera o programa biológico que favorece crescimento/progressão tumoral.
3) A evidência que sustenta o entusiasmo: o estudo INDIGO
O estudo que colocou o vorasidenibe no mapa foi o INDIGO, um ensaio clínico fase 3, randomizado, duplo-cego, controlado por placebo. Ele selecionou um cenário muito específico — e muito comum na vida real:
- Glioma de grau 2 com mutação IDH
- Doença residual ou recorrente após cirurgia
- Sem tratamento prévio além da cirurgia (isto é, sem rádio/quimioterapia antes do estudo)
- Objetivo clínico realista: ganhar tempo com segurança antes de precisar de terapias mais agressivas
Desfechos que importam na prática
O INDIGO avaliou:
- Sobrevida livre de progressão (PFS) por revisão independente
- Tempo até a próxima intervenção antineoplásica (por exemplo: iniciar radioterapia/quimioterapia ou nova estratégia)
Resultados principais (o “headline”)
- PFS mediana: 27,7 meses com vorasidenibe vs 11,1 meses com placebo
- Hazard ratio para progressão ou morte: 0,39
- Tempo até a próxima intervenção: também significativamente prolongado (HR 0,26)
Em linguagem de consultório: o remédio, em média, mais que dobrou o tempo sem progressão e adiou de forma robusta o momento de “subir o degrau” para RT/QT.
Uma observação metodológica importante
O estudo permitiu crossover (pacientes do placebo migravam para vorasidenibe após progressão). Isso é eticamente adequado, mas torna mais difícil responder, agora, a uma pergunta que todo mundo quer: qual será o impacto em sobrevida global no longo prazo? Esse é um ponto que ainda amadurece com seguimento.
4) Segurança: o que monitorar e como conversar com o paciente
Em neuro-oncologia, “tolerável” não é apenas “não grave”. É conviver por anos com um tratamento sem perder funcionalidade. Aqui, o vorasidenibe se mostrou viável para uso prolongado, com um alerta muito claro.
Principal ponto de atenção: fígado
O evento adverso mais característico é a elevação de transaminases (ALT/AST), podendo exigir pausa, redução de dose e, raramente, descontinuação.
O acompanhamento recomendado em bula inclui:
- Função hepática a cada 2 semanas nos 2 primeiros meses
- depois mensalmente (com um horizonte de acompanhamento prolongado, especialmente no início do uso)
Efeitos adversos mais comuns (visão geral)
Entre os mais frequentes aparecem sintomas como fadiga, cefaleia, diarreia, dor musculoesquelética, náusea e ocorrência de crises convulsivas (lembrando que crise pode ser também fenômeno do próprio tumor, e nem sempre é simples atribuir causalidade).
Interações e orientações práticas
A bula também chama atenção para interações metabólicas (ex.: via CYP1A2) e orienta evitar tabagismo por possível redução de concentração do fármaco, além de cuidados com anticoncepção (o medicamento pode reduzir eficácia de contraceptivos hormonais e há risco fetal).
5) Para quem, exatamente, esse remédio faz mais sentido?
Aqui está a parte mais “cirúrgica” do raciocínio: o vorasidenibe não substitui a cirurgia — ele se encaixa em um momento muito específico da jornada.
Em geral, ele conversa melhor com cenários como:
- Grau 2, IDH-mutante, após cirurgia (biópsia, ressecção subtotal ou total)
- Tumor predominantemente não realçante/indolente em imagem (um perfil típico de baixo grau)
- Situações em que a equipe está deliberadamente tentando postergar radioterapia e quimioterapia por impacto em qualidade de vida (especialmente em pacientes jovens e ativos)
- Pacientes com doença residual estável/recorrente em baixo volume, em que o “timing” de RT/QT é discutível
Para quem pode não ser o melhor primeiro passo
- Tumores com sinais de comportamento mais agressivo, crescimento acelerado, grande efeito de massa, deterioração neurológica rápida
- Cenários em que radioterapia/quimioterapia são necessárias de forma imediata por risco funcional
- Dúvidas diagnósticas relevantes: antes de “carimbar” um glioma como grau 2 IDH-mutante, precisamos de patologia e perfil molecular bem estabelecidos (incluindo, quando aplicável, codeleção 1p/19q, ATRX, TP53 etc.)
6) Como isso muda o “mapa mental” do tratamento em 2026?
Na prática, o vorasidenibe cria um novo degrau entre observar e irradiar/quimioterapizar:
Antes (simplificado):
Cirurgia → observar ou RT/QT (dependendo do risco) → progressão → nova intervenção
Agora (para um subgrupo bem definido):
Cirurgia → observar ou vorasidenibe → adiar RT/QT → manter função por mais tempo
Isso é particularmente relevante porque, em glioma de baixo grau, muitas vezes estamos tratando uma vida inteira, não apenas um tumor. A estratégia é: controlar sem “pagar” cedo demais o custo cognitivo e sistêmico das terapias clássicas.
7) Perguntas que eu mais ouço no consultório
“Isso cura o tumor?”
Não. A proposta realista é atrasar progressão e adiar terapias mais agressivas, mantendo qualidade de vida.
“Vou precisar de radioterapia mesmo assim?”
Muitos pacientes, em algum momento, ainda precisarão. O ganho está em quando e em quais condições chegaremos lá.
“Se eu fizer ressecção total, ainda faz sentido?”
Depende do risco biológico e do comportamento em seguimento. A discussão muda caso a caso, porque a decisão não é apenas “tomar ou não tomar”, e sim qual é a estratégia de tempo para aquela pessoa.
“Qual é o maior risco do remédio?”
Em termos práticos: alterações hepáticas, por isso a importância do monitoramento e de uma equipe habituada a conduzir dose, pausas e interações.
8) Próximos passos do campo: o que ainda precisamos aprender
O INDIGO abriu a porta; agora vêm as perguntas difíceis (e mais interessantes):
- Qual o impacto em sobrevida global com seguimento mais longo (especialmente considerando crossover)?
- Qual é o melhor momento de iniciar: logo após cirurgia vs. apenas quando houver crescimento mensurável?
- Como combinar com outras estratégias (ex.: timing de RT/QT, abordagens de preservação cognitiva, novos agentes)?
- Resistência e escape tumoral: quais mecanismos surgem e como contorná-los?
Em outras palavras: saímos do “funciona?” e entramos no “como usar do jeito mais inteligente?”.
Conclusão
O vorasidenibe representa uma mudança concreta na neuro-oncologia dos gliomas IDH-mutantes de grau 2 porque:
- trata um driver molecular relevante (IDH1/IDH2),
- é ativo no SNC,
- entrega um benefício clinicamente tangível: mais tempo sem progressão e mais tempo até a próxima intervenção.
Mas a palavra-chave é seleção. O melhor resultado aparece quando o medicamento é usado no paciente certo, no momento certo, dentro de um plano de longo prazo desenhado por equipe multidisciplinar (neurocirurgia, neuro-oncologia, radio-oncologia, neuropatologia, neurorradiologia).
Referências:
- Mellinghoff IK, et al. Vorasidenib in IDH1- or IDH2-Mutant Low-Grade Glioma. N Engl J Med. 2023;389:589–601. doi:10.1056/NEJMoa2304194. PubMed
- U.S. FDA. VORANIGO® (vorasidenib) – Prescribing Information (label). Initial U.S. Approval: 2024 (rev. 08/2024). FDA Access Data
- Mellinghoff IK, et al. Vorasidenib, a Dual Inhibitor of Mutant IDH1/2, in Recurrent or Progressive Glioma; Results of a First-in-Human Phase I Trial. Clin Cancer Res. 2021;27:4491–4499. MDPI
- Ballman KV, et al. Treatment of IDH-mutant glioma in the INDIGO era. npj Precision Oncology. 2024. Nature
- NCCN (via publicação de atualização). NCCN CNS Tumor Guidelines Update for 2024 (incorporação de dados do INDIGO em gliomas IDH-mutantes). PMC
- European Medicines Agency (EMA). Voranigo (vorasidenib) – EPAR/medicine overview; autorização na UE (17/09/2025). European Medicines Agency (EMA)
- ANVISA (Brasil). VORANIGO® (hemicitrato de vorasidenibe hemi-hidratado) – novo registro; indicação e publicação no DOU (11/08/2025). Serviços e Informações do Brasil
- Health Canada. Summary Basis of Decision – Voranigo (vorasidenib) (NOC em 27/08/2024). Portal de Saúde
- Reuters. US FDA approves Servier’s brain tumor treatment (aprovação FDA em 06/08/2024; dados de PFS do INDIGO). Reuters
- Observação: este texto é informativo e não substitui avaliação médica individualizada.