Em gliomas difusos IDH-mutantes de baixo grau (WHO grau 2), a cirurgia é mais do que “tirar um tumor”: ela é, muitas vezes, o primeiro determinante do tempo de controle da doença, do risco de transformação ao longo dos anos e da qualidade de vida — especialmente quando o paciente chega com crises epilépticas e preservação neurológica.
O ponto que a neurocirurgia moderna consolidou é simples de enunciar e complexo de executar: quanto maior a ressecção, melhor tende a ser o prognóstico — desde que seja uma ressecção máxima e segura, guiada por função.
A seguir, organizo o tema de forma metódica: o que significa “extensão de ressecção”, por que ela é prognóstica nos IDH-mutantes, como medimos isso hoje, quais dados sustentam o benefício e onde estão os limites do conceito.
1) O que exatamente chamamos de “extensão de ressecção” em baixo grau?
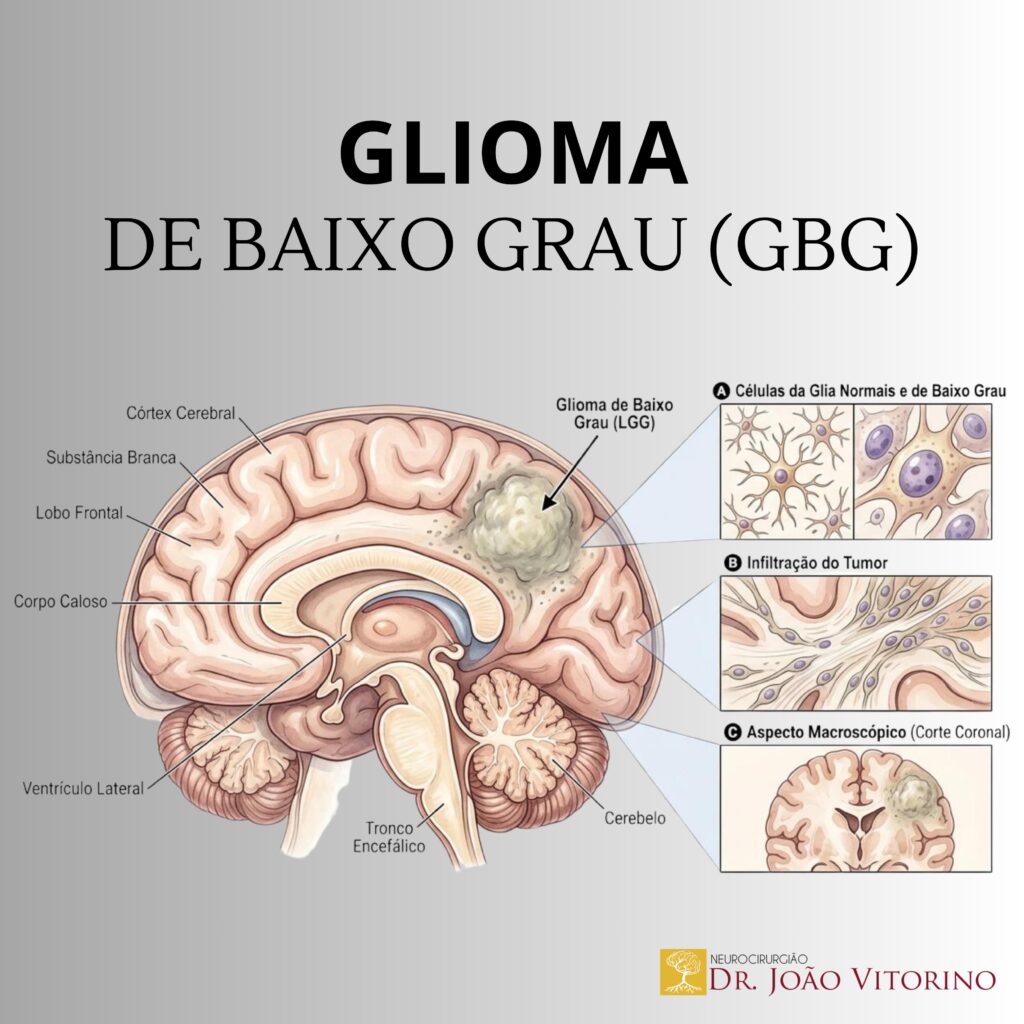
Nos gliomas de baixo grau IDH-mutantes, a “massa tumoral” costuma ser definida principalmente por hipersinal em T2/FLAIR (nem sempre há realce em T1 com contraste). Por isso, diferentemente do glioblastoma, onde o realce costuma orientar a meta cirúrgica, aqui a conversa é:
- Quanto do volume T2/FLAIR foi removido?
- Qual é o volume residual pós-operatório?
- A cirurgia foi uma biópsia, ressecção parcial, subtotal, quase total, total ou até supratotal/supramaximal (quando se vai além dos limites radiológicos mais aparentes em casos selecionados)?
A mensagem mais importante é que, em baixo grau, o “resíduo” medido no FLAIR tem peso prognóstico e tende a ser um marcador mais útil do que descrições subjetivas (“tirei quase tudo”).
2) Por que a ressecção é prognóstica em gliomas IDH-mutantes?
A) Redução de “carga biológica” ao longo de uma história natural longa
Gliomas IDH-mutantes de baixo grau frequentemente evoluem em anos. Mesmo com tratamentos adjuvantes quando indicados, o tumor é difuso e pode voltar a crescer a partir de células residuais. Assim, uma ressecção mais extensa pode:
- prolongar o tempo até progressão,
- reduzir a chance de transformação ao longo do tempo (dependendo do contexto),
- facilitar o controle de crises epilépticas,
- e, em muitos casos, adiar tratamentos com maior impacto neurocognitivo, como radioterapia, quando isso é clinicamente apropriado.
B) “Cirurgia guiada por função”: o benefício só vale se preserva autonomia
Não há ganho real em sobrevida se o paciente perde capacidade de trabalho, linguagem ou independência. Por isso, nos centros que trabalham com cirurgia acordada e mapeamento funcional, o objetivo é maximizar EOR com baixa taxa de déficits permanentes — e esse conceito influencia diretamente o prognóstico global “oncofuncional”.
3) O que a literatura contemporânea mostra
3.1. Diretrizes: extensão de ressecção como fator prognóstico e recomendação de “máxima ressecção segura”
Diretrizes europeias e consensos recentes reconhecem a EOR como variável associada a desfechos em gliomas e reforçam o princípio de maximal safe resection, incluindo nos IDH-mutantes. Em linhas gerais, a recomendação é clara: planejar ressecção ampla quando viável e segura, usando técnicas de preservação funcional.
3.2. Evidência populacional: ressecção precoce versus conduta expectante/“biopsiar e observar”
Um dos estudos mais citados no cenário IDH-mutante grau 2, com desenho populacional e seguimento prolongado, mostrou que ressecção precoce se associou a benefício sustentado de sobrevida, sem sinal de piora relevante de qualidade de vida relacionada à saúde no longo prazo. Na prática, esse trabalho deslocou o eixo da decisão: em muitos perfis, esperar “até piorar” deixa de ser o padrão.
3.3. “Quanto mais eu resseco” importa: volume residual e estratificação prognóstica
O avanço mais moderno não é apenas comparar “ressecou” versus “não ressecou”, mas medir quanto restou. Estudos recentes propõem e validam classificações padronizadas de extensão de ressecção para gliomas IDH-mutantes grau 2 e mostram um gradiente consistente: resíduos menores em T2/FLAIR se associam a melhores desfechos. Essa padronização é relevante porque reduz confusão entre centros e abre caminho para pesquisas mais comparáveis.
3.4. Ressecção supratotal/supramaximal: existe “algo além” da ressecção total?
Em casos selecionados — sobretudo tumores em regiões não eloquentes, com boa margem funcional — cresce o interesse em ressecções supratotais. Revisões e estudos de coorte sugerem que, para parte dos pacientes, ir além do “limite radiológico” pode melhorar controle e sobrevida, desde que a estratégia seja guiada por mapeamento e conectoma, não por agressividade cega. Ainda assim, é um campo onde a interpretação deve ser cuidadosa: há risco importante de viés de seleção (os tumores que permitem supratotal geralmente já são “mais ressecáveis”).
3.5. Oncofuncional: longuíssima sobrevida com preservação de vida real
Coortes com cirurgia acordada e mapeamento funcional em IDH-mutante grau 2 relatam sobrevidas medianas muito longas, frequentemente acima de 20 anos em alguns contextos, com manutenção de autonomia. E, dentro dessas séries, um padrão se repete: ressecções mais completas favorecem desfechos oncofuncionais (sobrevida + independência + cognição), e não apenas números de imagem.
4) O que limita a interpretação (e por que isso importa para o consultório)
Mesmo com dados fortes de associação, precisamos reconhecer as limitações:
- Viés de seleção: tumores menores, superficiais, não eloquentes e em pacientes jovens tendem a permitir EOR maior — e esses fatores por si só já melhoram prognóstico.
- Dificuldade de padronização: diferentes métodos de volumetria e timing da RM pós-op podem mudar a classificação de EOR.
- Heterogeneidade molecular dentro do “IDH-mutante”: astrocitoma IDH-mutante e oligodendroglioma (IDH-mutante, 1p/19q codeletado) têm histórias naturais diferentes; o “peso” da EOR pode variar entre subtipos.
- Interação com terapias adjuvantes: radioterapia/quimioterapia podem “compensar” parcialmente EOR menor em alguns cenários — mas isso não apaga a importância de operar bem quando é seguro.
O resultado prático: extensão de ressecção é prognóstica, mas a meta cirúrgica precisa ser individualizada.
5) Como eu traduzo isso em decisão cirúrgica (uma lógica simples e segura)
- Confirmar diagnóstico e subtipo molecular (IDH e, quando aplicável, 1p/19q).
- Mapear risco funcional (eloquência, fibras subcorticais, dominância, linguagem)
- Definir a meta realista: subtotal segura, total, ou supratotal selecionada.
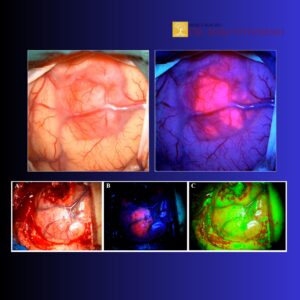
- Usar tecnologia a favor da função: cirurgia acordada quando indicada, mapeamento cortical/subcortical, neurofisiologia, navegação e estratégias de controle de crise.
- Pós-operatório precoce com RM e volumetria quando possível, para planejar seguimento e necessidade de adjuvância.
Conclusão
Em gliomas IDH-mutantes de baixo grau, a extensão de ressecção deixou de ser apenas um “detalhe cirúrgico” e passou a ser um marcador prognóstico robusto, com impacto real no curso da doença e na vida do paciente — especialmente quando falamos de ressecção precoce, menor volume residual em FLAIR e, em casos selecionados, ressecção supratotal guiada por função.
A regra que permanece inegociável é a mesma: máxima ressecção segura. A melhor cirurgia não é a mais radical; é a que entrega sobrevida com autonomia.
Referências
- Weller M, et al. EANO guidelines on the diagnosis and treatment of diffuse gliomas of adulthood. Nat Rev Clin Oncol. 2021.
- Goldbrunner R, et al. EANS–EANO guidelines on the extent of resection in gliomas. Neuro-Oncology. 2025.
- Jakola AS, et al. The impact of resection in IDH-mutant WHO grade 2 gliomas: a retrospective population-based parallel cohort study. J Neurosurg. 2022.
- Ng S, et al. Long-term autonomy, professional activities, cognition, and survival after awake functional-based resection in newly diagnosed IDH-mutant grade 2 glioma. Lancet EClinicalMedicine. 2024.
- Karschnia P, et al. Evidence-based recommendations on categories for extent of resection in glioma. Eur J Surg Oncol. 2021.
- Karschnia P, et al. A prognostic classification system for extent of resection in IDH-mutant grade 2 glioma: an international multicentre retrospective cohort study with external validation (RANO resect group). Lancet Oncology. 2025.
- Kreatsoulas D, et al. Supratotal Surgical Resection for Low-Grade Glioma. (Review) 2023.
- Gallotti AL, et al. Neuro-oncological superiority of supratotal resection in lower-grade gliomas. Neuro-Oncology. 2025.