Na cirurgia dos gliomas de alto grau, a meta é sempre a mesma: maximizar a ressecção com segurança funcional. Quanto maior a extensão de ressecção (EOR), melhores tendem a ser os desfechos oncológicos — desde que não se “pague” isso com déficit neurológico permanente. A fluorescência intraoperatória entrou nesse cenário como uma tentativa prática de responder à pergunta que todo neurocirurgião enfrenta no microscópio:
“Ainda tem tumor aqui… ou já é cérebro saudável?”
Hoje, duas estratégias dominam a prática clínica: 5-ALA (ácido 5-aminolevulínico) e fluoresceína sódica. Elas não são equivalentes; partem de princípios biológicos diferentes, têm limitações distintas e geram tipos de “verdade cirúrgica” diferentes.
1) Como cada técnica “enxerga” o tumor
5-ALA: fluorescência metabólica (mais “tumor-dirigida”)
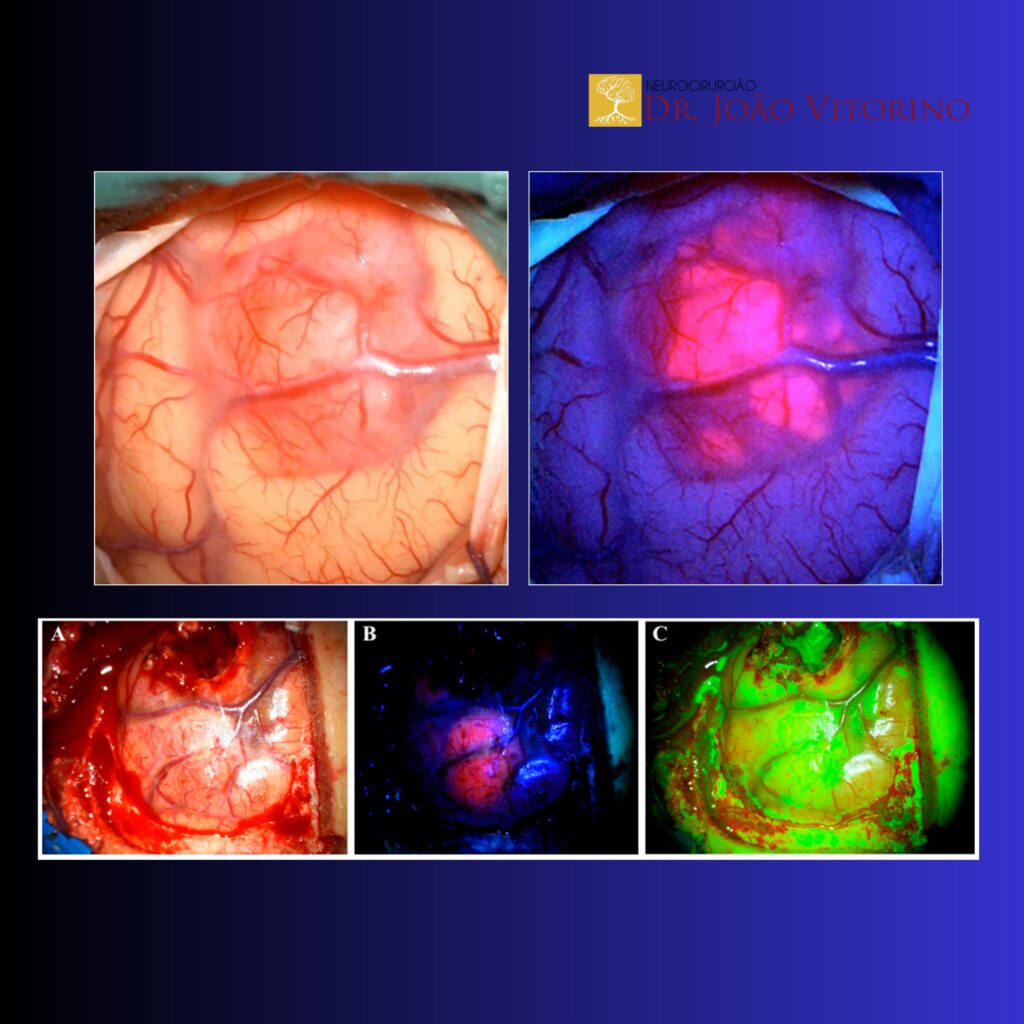
O 5-ALA é administrado por via oral algumas horas antes da cirurgia. Ele é convertido dentro das células em protoporfirina IX (PpIX), que se acumula em maior quantidade em muitos gliomas de alto grau. Quando iluminada com a luz adequada, essa PpIX emite fluorescência visível (geralmente em tons de rosa/vermelho).
Interpretação prática: o 5-ALA tende a marcar tecido tumoral viável, com uma relação mais direta com a biologia tumoral do que com a simples quebra de barreira hematoencefálica.
Ponto crítico: o sinal pode ser heterogêneo — e a ausência de fluorescência não garante ausência de infiltração microscópica.
Fluoresceína: fluorescência vascular (mais “BBB-dirigida”)
A fluoresceína é um corante intravenoso que extravasa onde há quebra da barreira hematoencefálica (BBB), o que é comum em áreas que realçam na RM com contraste. Em geral, usa-se um filtro específico no microscópio (ex.: YELLOW 560 nm) para melhor visualização.
Interpretação prática: a fluoresceína destaca regiões com permeabilidade vascular aumentada, frequentemente sobrepondo o realce por contraste.
Ponto crítico: por depender da BBB, ela pode marcar também tecidos não tumorais com inflamação, manipulação cirúrgica ou alterações vasculares. Ou seja, é mais suscetível a falso-positivo por “vazamento”.
2) O que a evidência sugere sobre “tirar mais tumor”
5-ALA: evidência mais madura e com ensaios randomizados
O 5-ALA tem o estudo clássico randomizado que mostrou aumento de ressecção completa do tumor contrastante e melhora em PFS, além de estudos mais recentes que reavaliaram seu impacto no contexto do tratamento contemporâneo (radioterapia + temozolomida). Em outras palavras: é a técnica com o “corpo” de evidência mais consolidado para gliomas de alto grau (1–3).
Fluoresceína: boa evidência para aumentar GTR, mas mais baseada em séries e meta-análises observacionais
Para fluoresceína, há meta-análises sugerindo aumento de taxa de ressecção completa em comparação com cirurgia sob luz branca, com resultados encorajadores — especialmente em centros que usam filtro e protocolos padronizados (4–6). Porém, a literatura é mais heterogênea em dose, filtro, critérios de “GTR” e tipo de tumor incluído.
3) E a comparação direta: 5-ALA versus fluoresceína
Aqui mora o ponto mais importante para quem lê “versus” no título:
- Ainda existem poucos estudos de comparação direta, cabeça-a-cabeça, com desenho robusto (idealmente randomizado).
- A maior parte das comparações vem de revisões sistemáticas e meta-análises que tentam padronizar resultados entre séries diferentes, ou de coortes retrospectivas.
O que essas sínteses sugerem, em linhas gerais:
- Ambas aumentam a taxa de ressecção extensa em gliomas de alto grau, quando comparadas à luz branca.
- O 5-ALA tende a apresentar vantagem em alguns desfechos oncofuncionais e consistência de evidência, mas a magnitude do benefício varia conforme a população, o método de avaliação de EOR e o quanto se consegue ressecar com segurança (7,8).
- A fluoresceína, por ser mais acessível e simples logisticamente, aparece como alternativa viável, sobretudo onde 5-ALA é caro ou indisponível; mas exige interpretação cuidadosa para não confundir extravasamento vascular com “tumor residual” (4–6).
4) Segurança e efeitos adversos: diferenças práticas do dia a dia
5-ALA
- Fotossensibilidade: o paciente precisa evitar luz intensa por um período após a administração.
- Exige logística pré-operatória (tempo correto de ingestão; checagem de contraindicações e interações).
Fluoresceína
- Geralmente bem tolerada em doses utilizadas para neurocirurgia, mas pode causar:
- náusea, urticária, reações alérgicas raras;
- coloração amarelada transitória de pele/urina.
- Depende de filtro adequado e padronização de dose/timing para reduzir “background” excessivo.
5) Onde cada técnica pode “falhar” (e como evitar armadilhas)
Armadilhas do 5-ALA
- Tumor pode ter fluorescência fraca ou ausente em áreas infiltrativas, especialmente nas margens.
- Sangue, necrose e iluminação podem dificultar leitura.
- A estratégia moderna combina 5-ALA com mapeamento funcional, neuronavegação e, quando disponível, ressonância intraoperatória.
Armadilhas da fluoresceína
- Como o sinal acompanha BBB, pode haver fluorescência em:
- áreas inflamatórias,
- tecido manipulado,
- regiões de extravasamento não neoplásico.
- A fluoresceína é ótima para “mapear” regiões de permeabilidade, mas exige que o cirurgião se pergunte sempre:
“Isso é tumor… ou é ‘efeito BBB’?”
6) Qual eu escolheria: um raciocínio cirúrgico objetivo
Em vez de “melhor” em abstrato, o que importa é melhor para este paciente, neste hospital, com esta equipe:
5-ALA tende a ser preferido quando:
- há acesso ao medicamento e ao microscópio com filtros adequados;
- o objetivo é maximizar a ressecção do componente tumoral viável contrastante com uma ferramenta de evidência mais consolidada;
- o caso será conduzido com mapeamento funcional e abordagem de “maximal safe resection”.
Fluoresceína tende a ser muito útil quando:
- há limitação de custo/disponibilidade do 5-ALA;
- busca-se uma ferramenta prática para realçar regiões com BBB alterada, especialmente em tumores contrastantes;
- há equipe habituada à interpretação e ao uso de filtros, com protocolo estável.
E o que realmente muda o jogo, independentemente do corante:
- cirurgia guiada por função (awake/monitorização quando indicada),
- estratégia de ressecção por planos anatômicos,
- controle hemostático e visibilidade,
- avaliação pós-operatória precoce de EOR,
- e integração com terapia adjuvante.
7) O futuro imediato: técnicas combinadas e “multi-modalidade”
Há um movimento crescente para sair do “ou… ou…” e entrar no “e…”:
- fluorescência + ultrassom intraoperatório,
- fluorescência + mapeamento avançado,
- e até estudos de dupla fluorescência em contextos específicos (embora isso ainda esteja mais explorado fora do HGG clássico) (9).
O caminho mais realista é: cada método enxerga uma dimensão diferente do tumor — e a cirurgia moderna é, cada vez mais, uma integração de camadas de informação.
Referências
- Stummer W, et al. Fluorescence-guided surgery with 5-aminolevulinic acid for resection of malignant glioma: a randomised controlled multicentre phase III trial. The Lancet Oncology. 2006.
- Picart T, et al. Use of 5-ALA fluorescence-guided surgery versus white-light conventional microsurgery for the resection of newly diagnosed glioblastomas (RESECT study): a French multicenter randomized phase III study. Journal of Neurosurgery. 2023.
- Stummer W, et al. Beyond fluorescence-guided resection: 5-ALA-based approaches as adjuncts to current standard therapy in glioblastoma. Acta Neurochirurgica. 2024.
- Smith EJ, et al. Fluorescein-Guided Resection of High Grade Gliomas: a meta-analysis. Clinical Neurology and Neurosurgery. 2021.
- Hamamcıoğlu MK, et al. The use of the YELLOW 560 nm surgical microscope filter for sodium fluorescein-guided resection of brain tumors. Clinical Neurology and Neurosurgery. 2016.
- Xiao Y, et al. Fluorescein-guided surgery in high-grade gliomas (eloquent and deep-seated regions). Journal of Cancer Research and Clinical Oncology. 2024.
- Kogias E, et al. 5-ALA vs. fluorescein guided resection for high-grade gliomas: a systematic review and meta-analysis. Molecular and Clinical Oncology. 2026.
- Palmieri G, et al. Fluorescence-Guided Surgery for High-Grade Gliomas: review (5-ALA and fluorescein). Surgical Innovation. 2021.
- Valerio JE, et al. Comparative Analysis of 5-ALA and Fluorescent Techniques in High-Grade Glioma Surgery: systematic review. 2025.